CUANTOS
En física, el término cuanto o cuantio (del latín Quantum, plural Quanta, que representa una cantidad de algo) denotaba en la física cuántica primitiva tanto el valor mínimo que puede tomar una determinada magnitud en un sistema físico, como la mínima variación posible de este parámetro al pasar de un estado discreto a otro.1 Se hablaba de que una determinada magnitud estaba cuantizada según el valor de cuanto. Es decir, cuanto es una proporción hecha por la magnitud dada.
Un ejemplo del modo en que algunas cantidades relevantes de un sistema físico están cuantizadas se encuentra en el caso de la carga eléctrica de un cuerpo, que sólo puede tomar un valor que sea un múltiplo entero de la carga del electrón. En la moderna teoría cuántica aunque se sigue hablando de cuantización el término cuanto ha caído en desuso. El hecho de que las magnitudes estén cuantizadas se considera ahora un hecho secundario y menos definitorio de las caracterísitcas esenciales de la teoría.
Los números cuánticos son unos números asociados a magnitudes físicas conservadas en ciertos sistemas cuánticos. Corresponden con los valores posibles de aquellos observablesque conmutan con el Hamiltoniano del sistema. Los números cuánticos permiten caracterizar los estados estacionarios, es decir los estados propios del sistema.
En física atómica, los números cuánticos son valores numéricos discretos que indican las características de los electrones en los átomos, esto está basado en la teoría atómica de Niels Bohr que es el modelo atómico más aceptado y utilizado en los últimos tiempos por su simplicidad.
En física de partículas, también se emplea el término números cuánticos para designar a los posibles valores de ciertos observables o magnitud física que poseen un espectro o rango posible de valores discretos.
I) El número cuántico principal n Este número cuántico está relacionado tanto con la energía como con la distancia media entre el núcleo y el electrón, medida en niveles energéticos, aunque la distancia media en unidades de longitud también crece monótonamente con n. Los valores de este número, que corresponde al número del nivel energético, varían teóricamente entre 1 e infinito, pero solo se conocen átomos que tengan hasta 8 niveles energéticos en su estado fundamental ya que el número atómico y el número cuántico principal se relacionan mediante 2n2 = Z < 110.
II) El número cuántico secundario o azimutal (l = 0,1,2,3,4,5,...,n-1), indica la forma de los orbitales y el subnivel de energía en el que se encuentra el electrón. Un orbital de un átomo hidrogenoide tiene l nodos angulares y n-1-l nodos radiales. Si:
l = 0: Subórbita "s" (forma circular) →s proviene de sharp (nítido) (*)
l = 1: Subórbita "p" (forma semicircular achatada) →p proviene de principal (*)
l = 2: Subórbita "d" (forma lobular, con anillo nodal) →d proviene de difuse (difuso) (*)
l = 3: Subórbita "f" (lobulares con nodos radiales) →f proviene de fundamental (*)
l = 4: Subórbita "g" (*)
l = 5: Subórbita "h" (*)
(*) Para obtener mayor información sobre los orbitales vea el artículo Orbital.
III) El número cuántico magnético (m, ml), Indica la orientación espacial del subnivel de energía, "(m = -l,...,0,...,l)". Para cada valor de l hay 2l+1 valores de m.
IV) El número cuántico de espín (s, ms), indica el sentido de giro del campo magnético que produce el electrón al girar sobre su eje. Toma valores ½ y -½.
RELATIVIDAD
La teoría de la relatividad incluye tanto a la teoría de la relatividad especial y como a la relatividad general, formuladas por Albert Einstein a principios del siglo XX, que pretendían resolver la incompatibilidad existente entre la mecánica newtoniana y el electromagnetismo.
La teoría de la relatividad especial, publicada en 1905, trata de la física del movimiento de los cuerpos en ausencia de fuerzas gravitatorias, en el que se hacían compatibles las ecuaciones de Maxwell del electromagnetismo con una reformulación de las leyes del movimiento.
La teoría de la relatividad general, publicada en 1915, es una teoría de la gravedad que reemplaza a la gravedad newtoniana, aunque coincide numéricamente con ella para campos gravitatorios débiles y "pequeñas" velocidades. La teoría general se reduce a la teoría especial en ausencia de campos gravitatorios.
No fue hasta el 7 de marzo de 2010 cuando fueron mostrados públicamente los manuscritos originales de Einstein por parte de la Academia Israelí de Ciencias, aunque la teoría se había publicado en 1905. El manuscrito contiene 46 páginas de textos y fórmulas matemáticas redactadas a mano, y fue donado por Einstein a laUniversidad Hebrea de Jerusalén en 1925 con motivo de su inauguración.
PREDECIBILIDAD
Predicción tiene por etimología el latín pre+dicere, esto es, “decir antes”. No se trata sólo de “decir antes”, sino de “decirlo bien”, o sea, acertar; también, hacerlo con un plazo suficiente para poder tomar las medidas que se crean oportunas, y además tener una idea de hasta cuándo es posible predecir el futuro con cierto éxito.
con cierto éxito.
 con cierto éxito.
con cierto éxito.
Cuando se efectúa una predicción , se está estimando un valor futuro de alguna variable que se considere representativa de una cierta situación.
, se está estimando un valor futuro de alguna variable que se considere representativa de una cierta situación.
 , se está estimando un valor futuro de alguna variable que se considere representativa de una cierta situación.
, se está estimando un valor futuro de alguna variable que se considere representativa de una cierta situación.
También se pueden hacer predicciones espaciales, como la ubicación, movilidad e intensidad local de fenómenos extremos, caso por ejemplo de los huracanes y tormentas tropicales
Normalmente ambos tipos de predicción están ligados y se realizan a la vez, como lo prueban los productos que ofrecen las s grandes agencias e institutos de Meteorología y Climatología.
Pueden construirse de modos muy diversos, de algunos de los cuales nos ocuparemos en este trabajo, y su bondad se mide -como es natural- por el porcentaje de aciertos en situaciones del pasado predichas con igual técnica. Las bases de registros disponibles hoy día permiten realizar experimentos de predecibilidad con datos pasados y simular situaciones ya conocidas mediante diversas técnicas, estudiando y comparando los resultados.
CAOS
Teoría del caos es la denominación popular de la rama de las matemáticas, la física y otras ciencias que trata ciertos tipos de sistemas dinámicos muy sensibles a las variaciones en las condiciones iniciales. Pequeñas variaciones en dichas condiciones iniciales pueden implicar grandes diferencias en el comportamiento futuro; complicando la predicción a largo plazo. Esto sucede aunque estos sistemas son en rigor determinismos es decir; su comportamiento puede ser completamente determinado conociendo sus condiciones iniciales.
Los sistemas dinámicos se pueden clasificar básicamente en:
Estables, Inestables, Caóticos.
Un sistema estable tiende a lo largo del tiempo a un punto, u órbita, según su dimensión (a tractor o sumidero). Un sistema inestable se escapa de los atractores. Y un sistema caótico manifiesta los dos comportamientos. Por un lado, existe un a tractor por el que el sistema se ve atraído, pero a la vez, hay "fuerzas" que lo alejan de éste. De esa manera, el sistema permanece confinado en una zona de su espacio de estados, pero sin tender a un a tractor fijo.
A tractores extraños
La mayoría de los tipos de movimientos mencionados en la teoría anterior suceden alrededor de a tractores muy simples, tales como puntos y curvas circulares llamadas ciclos límite. En cambio, el movimiento caótico está ligado a lo que se conoce como a tractores extraños, que pueden llegar a tener una enorme complejidad como, por ejemplo, el modelo tridimensional del sistema climático de Lorenz, que lleva al famoso a tractor de Lorenz conocidos, no sólo porque fue uno de los primeros, sino también porque es uno de los más complejos y peculiares, pues desenvuelve una forma muy peculiar más bien parecida a las alas de una mariposa.
EFECTO MARIPOSA La idea de la que parte la Teoría del Caos es simple: en determinados sistemas naturales, pequeños cambios en las condiciones iniciales conducen a enormes discrepancias en los resultados. Este principio suele llamarse efecto mariposa debido a que, en meteorología, la naturaleza no lineal de la atmósfera ha hecho afirmar que es posible que el aleteo de una mariposa en determinado lugar y momento, pueda ser la causa de un terrible huracán varios meses más tarde en la otra punta del globo.
RADIACTIVIDAD Y ÁTOMO
La radiactividad es una propiedad de ciertos elementos químicos cuyos núcleos atómicos son inestables: con el tiempo, para cada núcleo llega un momento en que alcanza su estabilidad al producirse un cambio interno, llamado desintegración radiactiva, que implica un desprendimiento de energía conocido de forma general como "radiación". La energía que interviene es muy grande si se compara con la desprendida en las reacciones químicas en que pueden intervenir las mismas cantidades de materiales, y el mecanismo por el cual se libera esta energía es totalmente diferente.
La radiactividad fue descubierta en 1896 por el químico francés Becquerel durante sus estudios sobre la fluorescencia. Observó que una placa fotográfica no expuesta a la luz y envuelta en papel negro era impresionada como por la luz visible o ultravioleta (o por los rayos X recientemente descubiertos por Röntgen), cuando el paquete se ponía en contacto con compuestos del elemento pesado uranio. Dedujo (correctamente) que este elemento debía producir algún tipo de radiación la cual atravesaba el papel hasta alcanzar y afectar a la emulsión fotográfica. Un cuidadoso estudio emprendido por Becquerel y otros científicos, entre ellos los Curie, Joliot, Soddy, Rutherford, Chadvick y Geiger, reveló que cierto número de elementos químicos pesados (muchos de ellos no descubiertos antes a causa de su rareza) parecían ser interiormente inestables y daban a origen a radiaciones penetrantes. Con ello, esos mismos elementos se transformaban en otros diferentes, siguiendo caminos complicados, pero bien definidos, en busca de una estabilidad final. Este fenómeno totalmente distinto de cualquier otro estudiado hasta entonces, recibió el nombre de radiactividad, y el proceso de transformación fue llamado desintegración radiactiva.
EL ÁTOMO NUCLEAR
Se define el número atómico del elemento como la cantidad de protones que contiene el núcleo en uno de sus átomos.
La masa atómica es el peso comparado de un núcleo atómico. Su unidad es la u.m.a (unidad de masa atómica) que se define como la doceava parte del peso del carbono –12. Un elemento es él y no otro por su número atómico. Así, el uranio lo es porque tiene 92 protones; si no fuera así dejaría de ser uranio. Sin embargo, un mismo elemento puede tener átomos de distinto número de neutrones. A los núcleos que tienen igual número de protones y distinto el de neutrones se les denominas isótopos. La existencia de isótopos de un mismo elemento es una razón por la que los pesos atómicos expresados en las tablas químicas no son números enteros.
Una anotación aceptada para indicar el número y la masa atómica de un núcleo es colocando la masa atómica en la parte superior izquierda del símbolo del elemento, y el número atómico en la inferior izquierda.
El número que indica la masa atómica se representa por A mayúscula y el que indica el número atómico se representa por una Z mayúscula.
Únicamente ciertas combinaciones de Z y A forman núcleos estables: si hay demasiados neutrones, o demasiados pocos, el núcleo sufrirá más pronto o más tarde un cambio, una desintegración radiactiva, que la llevará a la estabilidad en uno o varios pasos. El grado de es inestabilidad se pone de manifiesto por la energía emitida en la desintegración, así como en la velocidad de ésta. Tal velocidad de desintegración se mide por la vida media o período de semidesintegración, que es el tiempo necesario para que el número de átomos inicialmente presente se reduzca a la mitad por desintegración. Los tiempos de semidesintegración varían desde fracciones de segundo hasta millones de años. La desintegración radiactiva puede tener lugar de varias maneras diferentes.
Para ver el gráfico seleccione la opción "Descargar" del menú superior
Desintegración Alfa
Un núcleo demasiado pesado para ser estable expulsa un grupo compacto (una partícula alfa), consistente en dos protones, y dos neutrones, que deja al núcleo con una A cuatro unidades menor y una Z dos unidades más bajas, es decir, dos pasos atrás en la tabla periódica. Estructuralmente una partícula alfa es idéntica a un núcleo de Helio – 4. la desintegración alfa es frecuente entre los elementos naturales más pesados (uranio, polonio, y radio, por ejemplo), pero no conduce directamente a núcleos estables: antes se producen isótopos intermedios que experimentan nuevas desintegraciones.
Las partículas alfa tienen una energía de hasta 5.000.000 de electrovoltios, pero son tan voluminosas que sólo pueden atravesar unos 25 mm de aire y se ven detenidas por una simple hoja de papel o por la parte más externa de la piel humana. Sin embargo, por esta misma razón produce serios daños en el interior del cuerpo humano cuando son emitidas por materiales alfa – activos absorbidos inadvertidamente como polvo transportado por el aire, o través de heridas contaminadas. Los emisores naturales de partículas alfa, como el radio, son de uso práctico limitado, ahora que se dispone libremente de gran variedad de radioisótopos artificiales. No obstante, el uranio y su subproducto artificial, el plutonio (otro emisor alfa), son ambos fisibles y, por lo tanto, de importancia primordial en la producción de energía nuclear.
Desintegración Beta
Es un núcleo con demasiados neutrones, uno de estos puede transformarse en un protón más un electrón, que es expulsado en el núcleo. El electrón emitido de esta forma recibe el nombre de partícula β. El núcleo queda con una carga positiva más, con su Z en una unidad más alta y, por lo tanto, un lugar más arriba en la tabla periódica. Las partículas β son capaces de penetrar varios metros de aire, unos cuantos centímetros de tejido corporal o varios mm de metal o de plástico (que proporcionan un apantallamiento adecuado). Puede producir serias quemaduras superficiales o importantes daños internos sobre todo si son emitidos dentro del cuerpo durante periodos de tiempo algo prolongados. La desintegración β es el tipo mas frecuente de desintegración radiactiva tanto entre los isótopos artificiales como entre productos radiactivos procedentes de la desintegración alfa. Algunos de los radioisótopos artificiales obtenidos en aceleradores de partículas o separados en los productos de fisión formados en reactores nucleares tienen pocos neutrones, en lugar de demasiados. Estos se desintegran emitiendo positrones (partículas como los electrones pero cargadas positivamente), que se neutralizan casi de inmediato con los electrones ordinarios para producir una "radiación de aniquilación", con las cualidades de los rayos gamma. Los isótopos que emiten positrones tienen aplicaciones en diagnosis médica.
Emisión de rayos gamma
Esta emisión tiene lugar siempre que la desintegración beta no ha disipado suficiente energía para dar completa estabilidad al núcleo. Muchos isótopos naturales y artificiales con actividad alfa y beta son también emisores de rayos gamma. Los rayos gamma son una radiación electromagnética como los rayos X. Su intensidad se reduce al pasar a través de la materia en un grado que dependerá de su propia energía y de la densidad física del material absorbente. Los rayos gamma no son detenidos como las partículas alfa o beta, ni existen materiales opacos a ellos, como en el caso de la luz. Pueden necesitarse entre 5 y 25 centímetros de plomo o hasta 3 m de hormigón para conseguir una protección adecuada contra los rayos gamma de alta energía. El exceso de radiación gamma externa puede causar graves daños internos al organismo humano, peor no puede inducir radioactividad en él, ni en ningún otro material.
Otras formas de desintegración radiactiva son la transformación interna, en al que una reorganización interior del núcleo da como resultado la emisión de rayos X, o la captura de electrones, en la que un núcleo con demasiados protones captura un electrón de una orbita interna del propio átomo, convirtiendo así un protón en un neutrón, con emisión de rayos X y descenso de un lugar en la tabla periódica los núcleos de uranio – 235 y del U – 238 (emisores de partículas alfa), se desintegran alguna que otra vez por fisión nuclear espontánea, produciendo cualquier par de una gama de posibles núcleos de fisión, además de neutrones libres. El radioisótopo artificial californio – 252 se desintegra exclusivamente por fisión espontánea, proporcionando u8na fuente utilizable de neutrones. Unos pocos isótopos producto de fisión, en particular el yodo – 122, se desintegran con emisión retardada de neutrones poco después de haber sido formados y desempeñan un importante papel en el control de reactores.
La forma de desintegración, los tiempos de semidesintegración y las energías de emisión (energía máximas en el caso de partículas alfa y beta) son, en conjunto, características especificas que distinguen a un isótopo determinado y se pueden emplear para la identificación y medida de los propios emisores y, por tanto, de sus precursores, mediante la técnica deanálisis por activación.
VELOCIDAD DE DESINTEGRACIÓN
La velocidad de desintegración de un isótopo puede caracterizarse mediante una constante denominada período de semidesintegración, que se define como el espacio de tiempo que debe transcurrir que una determinada masa de isótopo se hayan desintegrado la mitad de los átomos que la forman. Esta constante tiene carácter estadístico, ya que es imposible predecir en que momento se va a producir la desintegración de un determinado átomo.
Otra constante que también se utiliza es la vida media que se define como el valor medio de la vida de los átomos del isótopo. No deben confundirse ambos conceptos, ya que ha menudo se utilizan de forma errónea.
FISIÓN NUCLEAR
Se entiende por fisión, la división de un núcleo muy pesado en un par de núcleos de masa próxima a 60, proceso en el cual se libera gran cantidad de energía
A finales de 1938, O.Hann y F. Strassmann descubrieron en uranio bombardeado con neutrones, la presencia del radioisótopo 139Ba, formado necesariamente por escisión del núcleo de uranio. Este proceso se denominó Fisión nuclear.
Según el modelo de la gota líquida, la fisión se produce porque al captar un neutrón, el núcleo oscila y se deforma, con lo que pierde su forma esférica adquiriendo la figura de un elipsoide entre cuyos extremos se produce una repulsión electrostática que puede llegar a provocar la rotura del núcleo pesado en dos fragmentos. En el caso del uranio-235, los fragmentos que se forman son núcleos de masas próximas a 95, el menor, y a 139, el mayor. Una reacción de fisión típica es:
235 1 90 144 1
29 0 38 54 0
Puesto que la relación neutrones/ protones es más elevada en el uranio que en los dos núcleos formados en la fisión, quedan dos neutrones en exceso que se liberan con gran energía. Si estos neutrones no son captados por núcleos de otros elementos y no escapan de la masa escindible, pueden provocar nuevas fisiones, siempre y cuando se hayan convertido en neutrones lentos mediante moderadores. Se logra así un proceso auto sostenido.
La energía liberada en la fisión de 1 g de uranio-235 es del orden de 108 kJ, es decir unos dos millones de veces la energía que se obtiene por combustión de 1 g de petróleo.
El primer reactor nuclear fue construido por Fermi en 1942, utilizando grafito como moderador. Así, los neutrones liberados al escindirse un núcleo de uranio-235 provocaban la escisión de nuevos núcleos de uranio-235 o la transmutación del uranio-238 en plutonio-239, que es así mismo fisionable.
En las bombas atómicas de fisión, la explosión se produce al unir dos masas de material fisionable de tamaño inferior al crítico. Es decir, que el recorrido medio que debe atravesar un neutrón liberado, en una fisión espontánea para provocar una nueva fisión, es mayor que el diámetro de esas masas. Al unirlas, se supera el tamaño crítico, con lo que se produce una reacción en cadena.
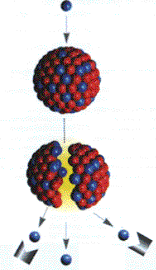
FUSIÓN NUCLEAR
En palabras sencillas, fusión nuclear es la unión de dos núcleos livianos acompañada por una liberación de energía.
Además de en la fisión de núcleos de átomos pesados, también se libera energía en la formación de núcleos intermedios a partir de núcleos muy ligeros, por ejemplo, de deuterio, 21H, y de tritio, 31H. Este proceso se conoce como fusión nuclear.
Una reacción de fusión típica es la unión de un núcleo del deuterio y uno de tritio para dar un núcleo de Helio y un neutrón:
2 3 4 1
1 1 2 0
Por gramo de combustible, esta reacción comporta la liberación de tres o cuatro veces más energía que una reacción de fisión. La energía liberada corresponde a la diferencia de masa entre el núcleo formado y sus constituyentes.
Las reacciones de fusión son las responsables de la energía que emiten el Sol y las estrellas, en cuyo interior la temperatura es del orden de 20 millones de grados y los átomos de hidrógeno están completamente ionizados. La energía emitida por el Sol equivale a la pérdida de una masa de 4,3 millones de toneladas en un segundo.
A diferencia de lo que ocurre con la fisión, los productos que se forman en las reacciones de fusión no son radiactivos y, además, los isótopos ligeros necesarios para la fusión son comunes (por ejemplo el deuterio existe en el mar), de ahí las grandes esperanzas depositadas en llegar a producir energía a partir de un proceso de fusión. El problema más importante planteado estriba en que los núcleos que se fusionan deben poseer suficiente energía para vencer las fuerzas electrostáticas de repulsión, lo que exige temperaturas de millones de grados. El material se hallará así en estado de plasma, y este plasma debe confinarse durante un tiempo suficientemente largo en un volumen no muy grande para que se produzca una reacción auto sostenida.
En las bombas termonucleares (bombas de hidrógeno) la temperatura necesaria se alcanza mediante la explosión de una o más bombas atómicas que actúan como detonantes de la fusión subsiguiente.

USOS DE LA RADIACTIVIDAD
El trazado isotópico en biología y en medicina
Los diferentes isótopos de un elemento tienen las mismas propiedades químicas. El reemplazo de uno por otro en una molécula no modifica, por consiguiente, la función de la misma. Sin embargo, la radiación emitida permite detectarla, localizarla, seguir su movimiento e, incluso, dosificarla a distancia. El trazado isotópico ha permitido estudiar así, sin perturbarlo, el funcionamiento de todo lo que tiene vida, de la célula al organismo entero. En biología, numerosos adelantos realizados en el transcurso de la segunda mitad del siglo XX están vinculados a la utilización de la radioactividad: funcionamiento del genoma (soporte de la herencia), metabolismo de la célula, fotosíntesis, transmisión de mensajes químicos (hormonas, neurotransmisores) en el organismo.
Los isótopos radioactivos se utilizan en la medicina nuclear, principalmente en las imágenes médicas, para estudiar el modo de acción de los medicamentos, entender el funcionamiento del cerebro, detectar una anomalía cardiaca, descubrir las metástasis cancerosas.
Las radiaciones y la radioterapia
Las radiaciones ionizantes pueden destruir preferentemente las células tumorales y constituyen una terapéutica eficaz contra el cáncer, la radioterapia, que fue una de las primeras aplicaciones del descubrimiento de la radioactividad.
En Francia, entre el 40 y el 50% de los cánceres se tratan por radioterapia, a menudo asociada a la quimioterapia o la cirugía. La radioactividad permite curar un gran número de personas cada año.
Las diferentes formas de radioterapia:
La curioterapia, utiliza pequeñas fuentes radioactivas (hilos de platino - iridio, granos de cesio) colocados cerca del tumor.
La tele radioterapia, consiste en concentrar en los tumores la radiación emitida por una fuente exterior.
La inmunorradioterapia, utiliza vectores radio marcados cuyos isótopos reconocen específicamente los tumores a los que se fijan para destruirlos.
La esterilización
La irradiación es un medio privilegiado para destruir en frío los microorganismos: hongos, bacterias, virus... Por esta razón, existen numerosas aplicaciones para la esterilización de los objetos, especialmente para el material médico-quirúrgico.
La protección de las obras de arte
El tratamiento mediante rayos gamma permite eliminar los hongos, larvas, insectos o bacterias alojados en el interior de los objetos a fin de protegerlos de la degradación. Esta técnica se utiliza en el tratamiento de conservación y de restauración de objetos de arte, de etnología, de arqueología.
La elaboración de materiales
La irradiación provoca, en determinadas condiciones, reacciones químicas que permiten la elaboración de materiales más ligeros y más resistentes, como aislantes, cables eléctricos, envolventes termo retractables, prótesis, etc.
La radiografía industrial X o g
Consiste en registrar la imagen de la perturbación de un haz de rayos X o g provocada por un objeto. Permite localizar los fallos, por ejemplo, en las soldaduras, sin destruir los materiales.
Los detectores de fugas y los indicadores de nivel
La introducción de un radioelemento en un circuito permite seguir los desplazamientos de un fluido, detectar fugas en las presas o canalizaciones subterráneas.
El nivel de un líquido dentro de un depósito, el espesor de una chapa o de un cartón en curso de su fabricación, la densidad de un producto químico dentro de una cuba... pueden conocerse utilizando indicadores radioactivos.
Los detectores de incendio
Una pequeña fuente radioactiva ioniza los átomos de oxígeno y de nitrógeno contenidos en un volumen reducido de aire. La llegada de partículas de humo modifica esta ionización. Por esta razón se realizan y se utilizan en los comercios, fábricas, despachos... detectores radioactivos sensibles a cantidades de humo muy pequeñas.
Las pinturas luminiscentes
Se trata de las aplicaciones más antiguas de la radioactividad para la lectura de los cuadrantes de los relojes y de los tableros de instrumentos para la conducción de noche.
La alimentación de energía de los satélites
Las baterías eléctricas funcionan gracias a pequeñas fuentes radioactivas con plutonio 239, cobalto 60 o estroncio 90. Estas baterías se montan en los satélites para su alimentación energética. Son de tamaño muy reducido y pueden funcionar sin ninguna operación de mantenimiento durante años.
La producción de electricidad
Las reacciones en cadena de fisión del uranio se utilizan en las centrales nucleares que, en Francia, producen más del 75% de la electricidad.
1. El ciclo del combustible nuclear
En un reactor, la fisión del uranio 235 provoca la formación de núcleos radioactivos denominados productos de fisión. La captura de neutrones por el uranio 238 produce un poco de plutonio 239 que puede proporcionar también energía por fisión.
Sólo una ínfima parte del combustible colocado en un reactor se quema en la fisión del núcleo. El combustible que no ha sido consumido y el plutonio formado se recuperan y se reciclan para producir de nuevo electricidad. Los otros elementos formados en el transcurso de la reacción se clasifican en tres categorías de residuos en función de su actividad, para ser embalados y luego almacenados.
2. La seguridad nuclear
La utilización de la fantástica fuente de energía contenida en el núcleo de los átomos implica el respeto riguroso de un conjunto de reglas de seguridad nuclear que permita asegurar el correcto funcionamiento de las centrales nucleares y la protección de la población.
3. Los residuos nucleares
Toda clase de actividad humana genera residuos. La industria nuclear no es una excepción a esta regla. Francia produce, de promedio, por año y por habitante:
5.000 Kg de residuos, de los cuales
100 Kg de residuos tóxicos, que incluyen
1 Kg de residuos nucleares de los cuales
5 gr de residuos son de alta actividad.
No sabemos aún destruir los residuos radioactivos. Su actividad disminuye naturalmente en el tiempo, más o menos rápido en función de su período. Deben utilizarse, por consiguiente, técnicas de confinamiento y de almacenamiento.
La reducción del volumen y de la actividad de los residuos radioactivos es, en Francia, un objetivo prioritario para la investigación. La amplitud del comportamiento a largo plazo de los residuos acumulados también es un eje primordial en la investigación
No hay comentarios.:
Publicar un comentario